
Indicaciones de uso de STELFONTA®
Tratamiento local aprobado por la EMA para el tratamiento de mastocitomas irresecables y no metastásicos.
Indicado para el tratamiento de:
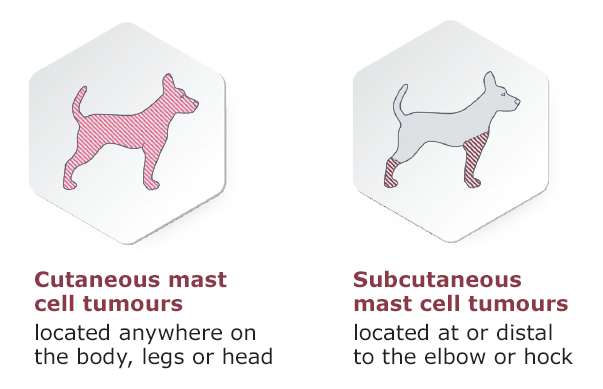
- Mastocitomas no metastásicos de cualquier grado
- Mastocitomas cutáneos
- Mastocitomas subcutáneos localizados en el codo, en el corvejón o distales a ellos
- Mastocitomas irresecables
Los tumores deben tener un volumen inferior o igual a 8 cm3 y deben ser accesibles a la inyección intratumoral.
4 pasos en el tratamiento de mastocitomas con STELFONTA®
La medicación concomitante prepara al paciente para el tratamiento con STELFONTA®
- Los mastocitos contienen gránulos que acumulan histamina y heparina, además de otros mediadores químicos.
- Cualquier manipulación de un mastocitoma puede causar una reacción de desgranulación del mismo. Este riesgo puede minimizarse asegurando la administración de medicación concomitante con corticosteroides, antagonistas de los receptores H1 y H2 tal como se indica en la etiqueta.
- La administración de corticosteroides se debe iniciar 2 días antes de la administración de STELFONTA® y se deben continuar diáriamente hasta 7 días post-tratamiento.
- Los antagonistas de los receptores H1 y H2 se deben iniciar el día de la administración de STELFONTA® y continuar durante 8 días.
- No se requiere ni sedación ni ninguna otra medicación*.
* Los perros sometidos a tratamiento con el producto deben estar adecuadamente sujetos, incluso mediante sedación si es necesario

Consejo experto de
Dr. Justine Campbell
No tengas la tentación de prescindir de la medicación concomitante; es esencial para el protocolo y la clave para prevenir los posibles síntomas sistémicos asociados a la desgranulación del mastocitoma.
Calendario de dosificación de la medicación concomitante
Inyección de STELONTA®
- Día
- Día
- Día
- Día
- Día
- Día
- Día
- Día
- Día
- Día
- Día
Periodo de posibles manifestaciones clínicas a causa de la desgranulación
Antagonistas de los receptores H1 y H2
Corticosteroides
Por ejemplo, prednisona o prednisolona; 0,5 mg/kg PO BID
Corticosteroides
0,5 mg/kg PO SID
Analgesia
A discreción del veterinario (no AINEs)
BID: dos veces al día; SID: una vez al día; PO: vía oral.
La destrucción del tumor indica que STELFONTA® está funcionando
Comienza el efecto oncolítico e inflamatorio.
Horas previstas: STELFONTA® comienza a actuar, con cambios visibles en el lugar del tumor. Las células del tumor y los vasos sanguíneos tumorales comenzarán a destruirse, lo que provocará un cambio de color en el tumor y una hinchazón en el lugar del tratamiento.
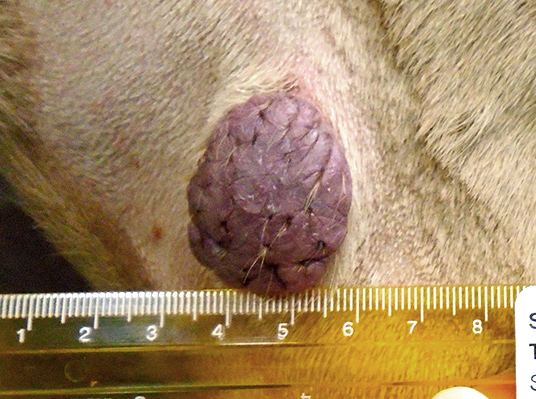
Mayor permeabilidad de la vasculatura tumoral.
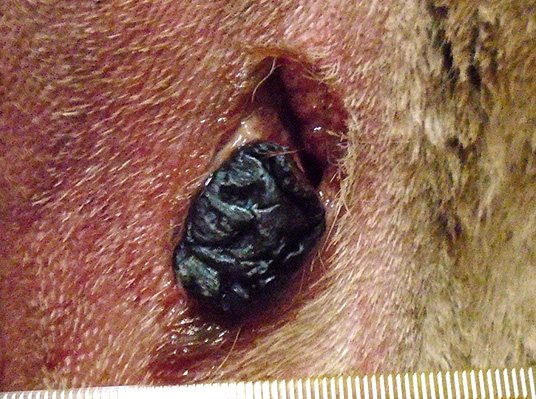
Días previstos: El tumor puede volverse negro. La superficie puede volverse blanda y el líquido puede filtrarse del tumor a medida que continúa descomponiéndose. La hinchazón en el sitio de tratamiento puede continuar y causar algunas molestias al perro.

Consejo experto de
Dr. Justine Campbell
La presencia prolongada de tejido tumoral puede ralentizar el proceso de cicatrización de la herida, por lo que no es perjudicial si el perro se lame la herida.
Dependiendo del tamaño del tumor y de la cantidad de tejido necrótico, puede aparecer un mal olor alrededor de los días 3 y 6 después del tratamiento.
Curación sin manipulación* por segunda intención con con la mínima intervención
- A medida que el tumor vaya destruyéndose, puede formarse un defecto o ‘bolsillo’ donde estaba el tumor
- Se observará una capa de nuevo tejido de granulación, indicativa de la cicatrización por segunda intención
- Cubrir el punto de aplicación el primer día tras el tratamiento para prevenir el contacto directo con residuos de la herida o fugas de producto
- El 96% de las áreas tumorales cicatrizadas a los 84 días
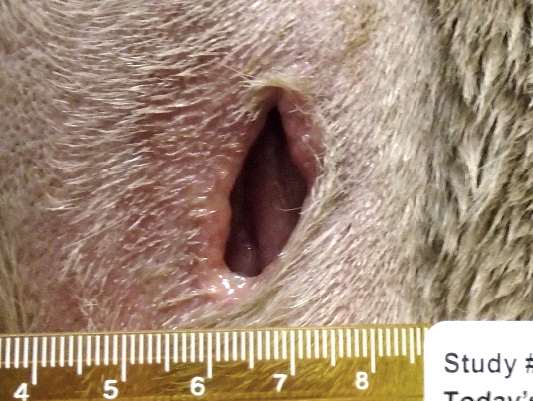
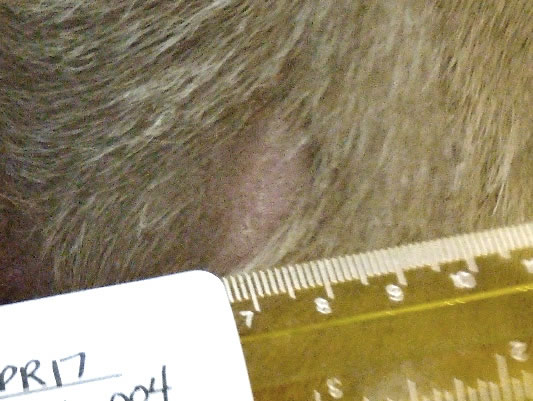
* Intervención mínima. Cubrir el punto de aplicación el primer día tras el tratamiento para prevenir el contacto directo con residuos de la herida o fugas de producto.
En caso que se requiera un segundo tratamiento con STELFONTA
- En los estudios clínicos, el 75% de los tumores fueron eliminados con un solo tratamiento de STELFONTAMelo SR, et al. Veterinary Cancer Society, Houston, Texas, USA.
- Si aún queda tejido tumoral 4 semanas después del tratamiento inicial y la superficie de la masa residual está intacta, se puede administrar una segunda dosis. Se debe medir el tamaño del tumor residual y calcular la nueva dosis antes de administrar la segunda dosis.
El mecanismo de acción (MoA) de STELFONTA® hace que las reacciones comunes sean predecibles
- Las reacciones adversas más comunes tales como dolor, hematoma, eritema o edema en el lugar de inyección, cojera en la extremidad tratada y formación de heridas, están relacionados con el MoA de STELFONTA® en el lecho tumoral.
- La formación de heridas se produce por segunda intención tras el tratamiento con STELFONTA®.
Efectos adversos esperados tras el tratamiento con STELFONTA®:
- Signos debidos al mecanismo de acción incluyen:
-
-
Formación de herida en el punto de inyección seguido de necrosis tumoral
-
Hematoma, eritema o edema en el lugar de inyección
-
Dolor en el punto de inyección
-
Cojera en la extremidad tratada
-
Agrandamiento de los nódulos linfáticos regionales
-
- Signos debidos a la medicación concomitante:
-
- Poliuria
- Polidipsia
- Taquipnea
- Incremento del apetito
- Elevación de la fosfatasa alcalina
- Signos de desgranulación:
-
- Vómitos
- Diarreas
- Letargo
- Anorexia/hiporexia
- Alteración de la respiración/taquipnea
- Urticaria, hematoma y edema en el punto de tratamiento o lejos de este
- Taquicardia
- Hipotensión
Para información sobre contraindicaciones y advertencias,
por favor, consulte la Ficha Técnica del Producto


