El uso de HCA y ciclosporina en la dermatitis por hipersensibilidad no alimentaria ni DAPP
HISTORIAL Y EXAMEN CLÍNICO

Una gata de 4 años, castrada y de pelo corto doméstico, se presentó con una historia de dos años de pododermatitis recurrente y autotraumatismo que afectaba a las cuatro extremidades. Por lo demás, la gata gozaba de buena salud, estaba al día con las vacunas rutinarias y se alimentaba con un pienso comercial equilibrado. No había antecedentes de viajes y el gato vivía predominantemente en el interior, con acceso ocasional al jardín.
El tratamiento repetido con acetato de metilprednisolona de depósito de 4mg/kg y cefovecina de 8mg/kg no había logrado controlar completamente los signos clínicos del gato.
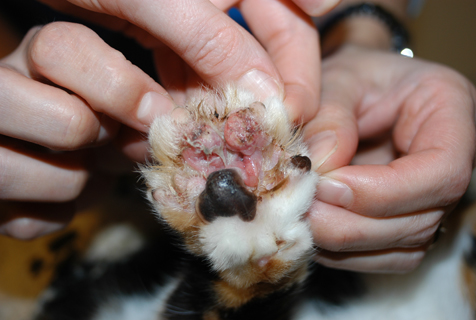
La exploración física general no presentaba ninguna anomalía. El examen dermatológico reveló una placa bien delimitada, alopécica, eritematosa y ulcerada presente en la cara palmar de la extremidad torácica derecha entre los dedos dos y cuatro (figura 1). La piel pedal circundante de la pata estaba húmeda y eritematosa. También había pequeñas erosiones que afectaban al labio superior adyacente a los dientes caninos (figura 2).
DIAGNÓSTICO DIFERENCIAL
-
Los diagnósticos diferenciales de la lesión pedal incluyen:
-
Placa eosinofílica (PE),
-
Neoplasia (carcinoma de células escamosas, linfoma, mastocitoma),
-
Enfermedad vírica cutánea (viruela bovina felina, herpes virus, calici virus),
-
Infección por micobacterias,
-
Infección fúngica profunda,
-
Foliculitis bacteriana y furunculosis,
-
Reacción a cuerpo extraño,
-
Enfermedad nodular estéril.
-
-
Los diagnósticos diferenciales para la lesión labial incluyen:
-
Úlcera eosinofílica leve (indolente)
-
Traumatismo
-
Teniendo en cuenta la edad del gato, el aspecto clínico de la lesión pedal y la presencia de prurito, se sospechó la existencia de una PE. Dado que las dermatitis eosinofílicas se observan con frecuencia en las enfermedades alérgicas de la piel y que los signos clínicos de la gata cumplían 5/8 de los criterios de Favrot para los gatos que presentan prurito, se hizo un diagnóstico provisional de dermatitis por hipersensibilidad felina (DH).1,2,3
DIAGNÓSTICO

TRATAMIENTO
 Se sospechó que la infección bacteriana estafilocócica era secundaria a la inflamación asociada a la enfermedad alérgica de la piel; ésta se trató con 8 mg/kg de cefovecina durante cuatro semanas. La gravedad de la PE del gato justificaba un tratamiento sintomático antes de completar las pruebas diagnósticas, por lo que se administró dexametasona a razón de 0,08 mg/kg PO SID 7 días y luego EOD 7 días y dos veces por semana durante 2 semanas. Este tratamiento fuera de licencia se utilizó porque el propietario no podía administrar comprimidos y ofrecía una mayor flexibilidad de dosificación con un control a corto plazo de la enfermedad clínica, en comparación con las formulaciones de esteroides de depósito y otros fármacos inmunomoduladores autorizados. Se evitó el uso extensivo de este potente glucocorticoide debido al riesgo de efectos adversos. Las lesiones del gato se resolvieron, pero a pesar de los ensayos continuos de control de alimentos y ectoparásitos, la inflamación eosinofílica estéril reapareció cuando se suspendió el tratamiento, por lo que se diagnosticó una dermatitis por hipersensibilidad no alimentaria (DH).4
Se sospechó que la infección bacteriana estafilocócica era secundaria a la inflamación asociada a la enfermedad alérgica de la piel; ésta se trató con 8 mg/kg de cefovecina durante cuatro semanas. La gravedad de la PE del gato justificaba un tratamiento sintomático antes de completar las pruebas diagnósticas, por lo que se administró dexametasona a razón de 0,08 mg/kg PO SID 7 días y luego EOD 7 días y dos veces por semana durante 2 semanas. Este tratamiento fuera de licencia se utilizó porque el propietario no podía administrar comprimidos y ofrecía una mayor flexibilidad de dosificación con un control a corto plazo de la enfermedad clínica, en comparación con las formulaciones de esteroides de depósito y otros fármacos inmunomoduladores autorizados. Se evitó el uso extensivo de este potente glucocorticoide debido al riesgo de efectos adversos. Las lesiones del gato se resolvieron, pero a pesar de los ensayos continuos de control de alimentos y ectoparásitos, la inflamación eosinofílica estéril reapareció cuando se suspendió el tratamiento, por lo que se diagnosticó una dermatitis por hipersensibilidad no alimentaria (DH).4
Se inició un tratamiento a largo plazo con ciclosporina 7 mg/kg PO SID. Se ha demostrado que la ciclosporina a esta dosis es un tratamiento seguro y eficaz para la DH felina no relacionada con las pulgas ni con los alimentos, incluidos los gatos que presentan PE.5 Los signos clínicos del gato mejoraron con este tratamiento, pero el propietario tuvo problemas con la administración y la lesión pedal no se resolvió por completo. Por lo tanto, se introdujo un spray tópico de HCA simultáneo. Se aplicaron dos pulverizaciones en la piel afectada durante 7 días (figura 3) y luego se redujo el tratamiento a días alternos y dos veces por semana para el tratamiento de mantenimiento.

DISCUSIÓN
El aceponato de hidrocortisona (HCA) está autorizado para el tratamiento de la dermatitis atópica canina en forma de spray al 0,0584%.6 La aplicación diaria o en días alternos ha demostrado ser eficaz en el tratamiento de gatos con PE en un pequeño estudio.7 Además, el tratamiento proactivo en dos días consecutivos cada semana ha demostrado ser eficaz y bien tolerado en el tratamiento a largo plazo de la dermatitis atópica canina.8 Los posibles brotes de la enfermedad asociados a los ectoparásitos se gestionaron mediante la continuación de la selamectina tópica cada cuatro semanas y el tratamiento del entorno dos veces al año con permetrina / piriproxifeno / butóxido de piperonilo combinados.

1. Bloom, P.B. (2006). Canine and feline eosinophilic skin diseases, Veterinary Clinics of North America Small Animal Practice, 36(1), p141-60.
2. Taglinger, K., Day, M.J. & Foster, A.P. (2007). Characterization of inflammatory cell infiltration in feline allergic skin disease, Journal of Comparative Pathology, 137(4), p211-23.
3. Favrot, C., Steffan, J., Seewald, W., Hobi, S., Linek, M., Marignac, G., Olivry, T., Beco, L., Nett, C., Fontaine, J. & Roosje, P. (2012). Establishment of diagnostic criteria for feline non flea-induced hypersensitivity dermatitis, Veterinary Dermatology, 23(1), p45–50.
4. Favrot, C. (2013). Feline non-flea induced hypersensitivity dermatitis clinical features, diagnosis and treatment, Journal of Feline Medicine and Surgery, 15(9), p778–84.
5. Roberts, E.S. et al (2016) ‘Confirmatory field study for the evaluation of ciclosporin at a target dose of 7.0 mg/kg (3.2 mg/lb) in the control of feline hypersensitivity dermatitides’. Journal of Feline Medicine and Surgery, 18(11), p889-97.
6. Nuttall, T., Mueller, R., Bensignor, E., Verde, M., Noli, C., Schmidt, V. & Rème, C. (2009) Efficacy of a 0.0584% hydrocortisone aceponate spray in the management of canine atopic dermatitis: a randomised, double blind, placebo-controlled trial, Veterinary Dermatology, 20(3), p191-8.
7. Schmidt, V., Buckley, L.M., McEwan, N.A., Reme, C.A. & Nuttall, T.J. (2012). Efficacy of a 0.0584% hydrocortisone aceponate spray in presumed feline allergic dermatitis: an open label pilot study, Veterinary Dermatology, 23(1), p11-6.
8. Lourenço, A.M., Schmidt, V., Sao Braz, B., Nobrega, D., Nunes, T., Duarte‐Correia, J.H., Matias, D., Maruhashi, E., Reme, C.A. & Nuttall, T. (2016). Efficacy of proactive long-term maintenance therapy of canine atopic dermatitis with 0.0584% hydrocortisone aceponate spray: a double-blind placebo controlled pilot study, Veterinary Dermatology, 27(2), p88-92.
9. Bryan, J. & Frank, L.A. (2010). Food allergy in the cat: a diagnosis by elimination, Journal of Feline Medicine and Surgery, 12(11), p861-6.

